
Bloque
de la tabla periódica

CLASIFICACIÓN DE
LOS ELEMENTOS DE LA TABLA PERIÓDICA
La primera clasificación de elementos conocida, fue propuesta por Antoine
Lavoisier, quien propuso que los elementos se clasificaran
en metales, no metales y metaloides o metales de
transición. Aunque muy práctico y todavía funcional en la tabla periódica
moderna, fue rechazada debido a que había muchas diferencias tanto en
las propiedades físicas como en las químicas.
· Antoine-Laurent
de Lavoisier químico, biólogo y economista francés, considerado
el creador de la química moderna, junto a su esposa, la
científica Marie-Anne Pierrette Paulze, por sus estudios sobre la
oxidación de los cuerpos, el fenómeno de la respiración animal,
el análisis del aire,
la ley de conservación de la masa o ley Lomonósov-Lavoisier,
la teoría calórica y la combustión.
· Se llama metales a
los elementos químicos caracterizados por ser buenos conductores
del calor y
la electricidad.
Poseen alta densidad y
son sólidos en temperaturas normales (excepto el mercurio); sus sales
forman iones electropositivos (cationes) en disolución.
Los metales los solemos clasificar de la siguiente forma:
· Metales
reactivos. Se denomina así a los elementos de las dos primeras columnas
(alcalinos y alcalinotérreos) al ser los metales más reactivos por regla
general.
· Metales de
transición. Son los elementos que se encuentran entre las columnas largas,
tenemos los de transición interna (grupos cortos) y transición externa o
tierras raras (lantánidos y actínidos).
· Otros metales.
Son los que se encuentran en el resto de grupos largos. Algunos de ellos tienen
propiedades de no metal en determinadas circunstancias (semimetales o
metaloides).
· Propiedades
de los metales.
Por regla general los metales tienen las siguientes propiedades:
· Son buenos
conductores de la electricidad.
· Son buenos
conductores del calor.
· Son
resistentes y duros.
· Son brillantes
cuando se frotan o al corte.
· Son maleables, se
convierten con facilidad en láminas muy finas.
· Son dúctiles, se
transforman con facilidad en hilos finos.
· Se producen
sonidos característicos (sonido metálico)
cuando son golpeados.
· Tienen altos
puntos de fusión y
de ebullición.
· Poseen elevadas
densidades; es decir, tienen mucha masa para su tamaño: tienen muchos átomos
juntos en un pequeño volumen.
Propiedades de los no metales:
· Son malos
conductores de la electricidad.
· Son malos
conductores del calor.
· Son poco
resistentes y se desgastan con facilidad.
· No reflejan
la luz como
los metales, no tienen el denominado brillo metálico. Su superficie no es tan
lisa como en los metales.
· Son frágiles, se
rompen con facilidad.
· Tienen
baja densidad.
· No son atraídos
por los imanes.
· Tienen tendencia
a formar iones negativos.
Hay algunas excepciones a las
propiedades generales enunciadas anteriormente:
· El diamante es un
no metal pero presenta una gran dureza.
· El grafito es un
no metal pero conduce la electricidad.
·
No Metales, Metales y Metaloides de la tabla periódica:


Enlaces
Químicos
Son la unión de átomos que forma
moléculas existen 3 tipos de enlaces:

1. Enlaces Iónicos
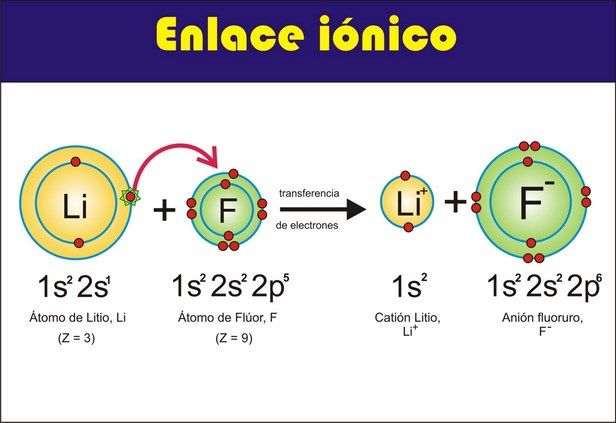
2. Enlace Metálicos
3.
Enlace Covalentes


No hay comentarios:
Publicar un comentario